- Autora Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:34.
- Última modificació 2025-06-01 07:36.
La diferència clau entre l'àcid carbònic i el bicarbonat és que l'àcid carbònic és un compost químic neutre, mentre que el bicarbonat és un compost químic carregat negativament.
L'àcid carbònic és un àcid feble que es forma en solució quan el diòxid de carboni es dissol a l'aigua, amb la fórmula química H2CO3. El bicarbonat es forma per la combinació de tres àtoms d'oxigen, un àtom d'hidrogen i un àtom de carboni amb la fórmula química HCO3-.
Què és l'àcid carbònic?
L'àcid carbònic és H2CO3. De vegades, donem aquest nom a solucions que tenen diòxid de carboni dissolt en aigua o aigua carbonatada. Això es deu al fet que l'aigua carbonatada conté una petita quantitat de H2CO3. A més, l'àcid carbònic és un àcid feble, i pot formar dos tipus de sals com els carbonats i els bicarbonats. La massa molar d'aquest compost és de 62,024 g/mol.
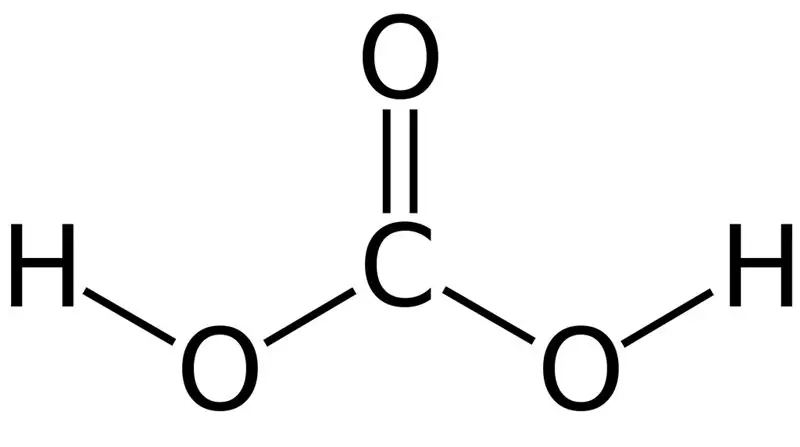
Figura 01: l'estructura química de l'àcid carbònic
Quan el diòxid de carboni es dissol a l'aigua, entra en equilibri entre el diòxid de carboni i l'àcid carbònic. L'equilibri és el següent:
CO2 + H2O ⟷ H2CO3
Si a una base afegim un excés d'àcid carbònic, dóna bicarbonat. Però, si hi ha un excés de base, l'àcid carbònic tendeix a donar sals carbonatades. Més precisament, l'àcid carbònic és un compost d'àcid carboxílic que té dos substituents del grup hidroxil units al carboni carbonílic. A més, és un àcid polipròtic, que és capaç de donar protons. Té dos protons extraïbles, de manera que és específicament dipròtic.
Què és el bicarbonat?
El bicarbonat es forma per la combinació de tres àtoms d'oxigen, un àtom d'hidrogen i un àtom de carboni. El producte d'aquesta combinació pot ser un ió o un compost amb més electrons que protons. La podem descriure com una espècie química que té la fórmula química HCO3-.
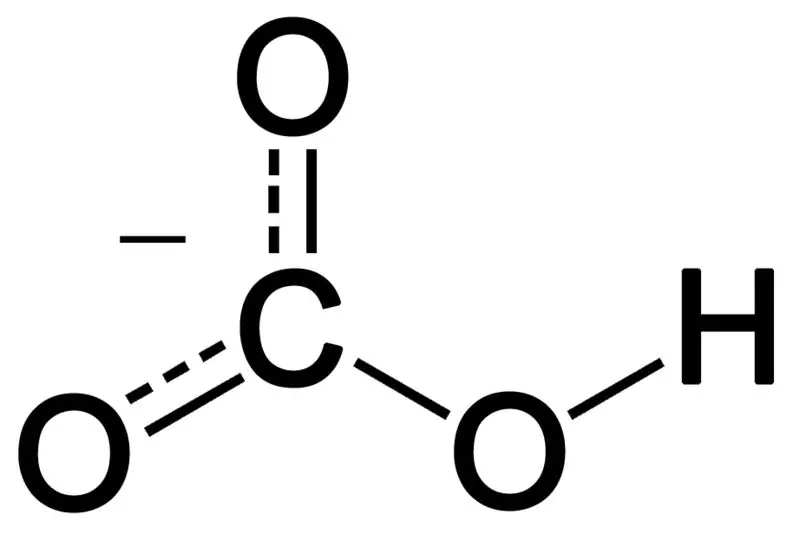
Figura 02: l'estructura química de l'anió bicarbonat
Aquest compost és una part crucial del sistema amortidor del pH del cos, en termes senzills: és responsable de mantenir la sang en un estat que no sigui massa àcid ni massa bàsic. A més, serveix com a forma de controlar els sucs digestius un cop l'estómac ha acabat de digerir els aliments. A més, l'àcid carbònic de l'aigua de pluja forma ions bicarbonat quan colpeja les roques. Aquest flux d'ions bicarbonat és important per mantenir el cicle del carboni en marxa.
Quina diferència hi ha entre l'àcid carbònic i el bicarbonat?
L'àcid carbònic és un àcid feble que es forma en solució quan el diòxid de carboni es dissol a l'aigua, i la seva fórmula química és H2CO3. El bicarbonat es forma per la combinació de tres àtoms d'oxigen, un àtom d'hidrogen i un àtom de carboni amb la fórmula química HCO3-. La diferència clau entre l'àcid carbònic i el bicarbonat és que l'àcid carbònic és un compost químic neutre, mentre que el bicarbonat és un compost químic carregat negativament. A més, l'àcid carbònic s'utilitza en l'elaboració de begudes amb bombolles, gasoses, tractament de dermatitis, en col·lutoris, etc., mentre que el bicarbonat s'utilitza en preparacions alimentàries com la cocció (com a agent llevat), i li dóna la capacitat de resistir els canvis de pH.
La següent infografia resumeix la diferència entre l'àcid carbònic i el bicarbonat en forma de taula per comparar-les.
Resum: àcid carbònic vs bicarbonat
L'àcid carbònic és H2CO3. El bicarbonat es forma per la combinació de tres àtoms d'oxigen, un àtom d'hidrogen i un àtom de carboni, amb la fórmula química HCO3-. La diferència clau entre l'àcid carbònic i el bicarbonat és que l'àcid carbònic és un compost químic neutre, mentre que el bicarbonat és un compost químic carregat negativament.






